质粒放行检项目
收起
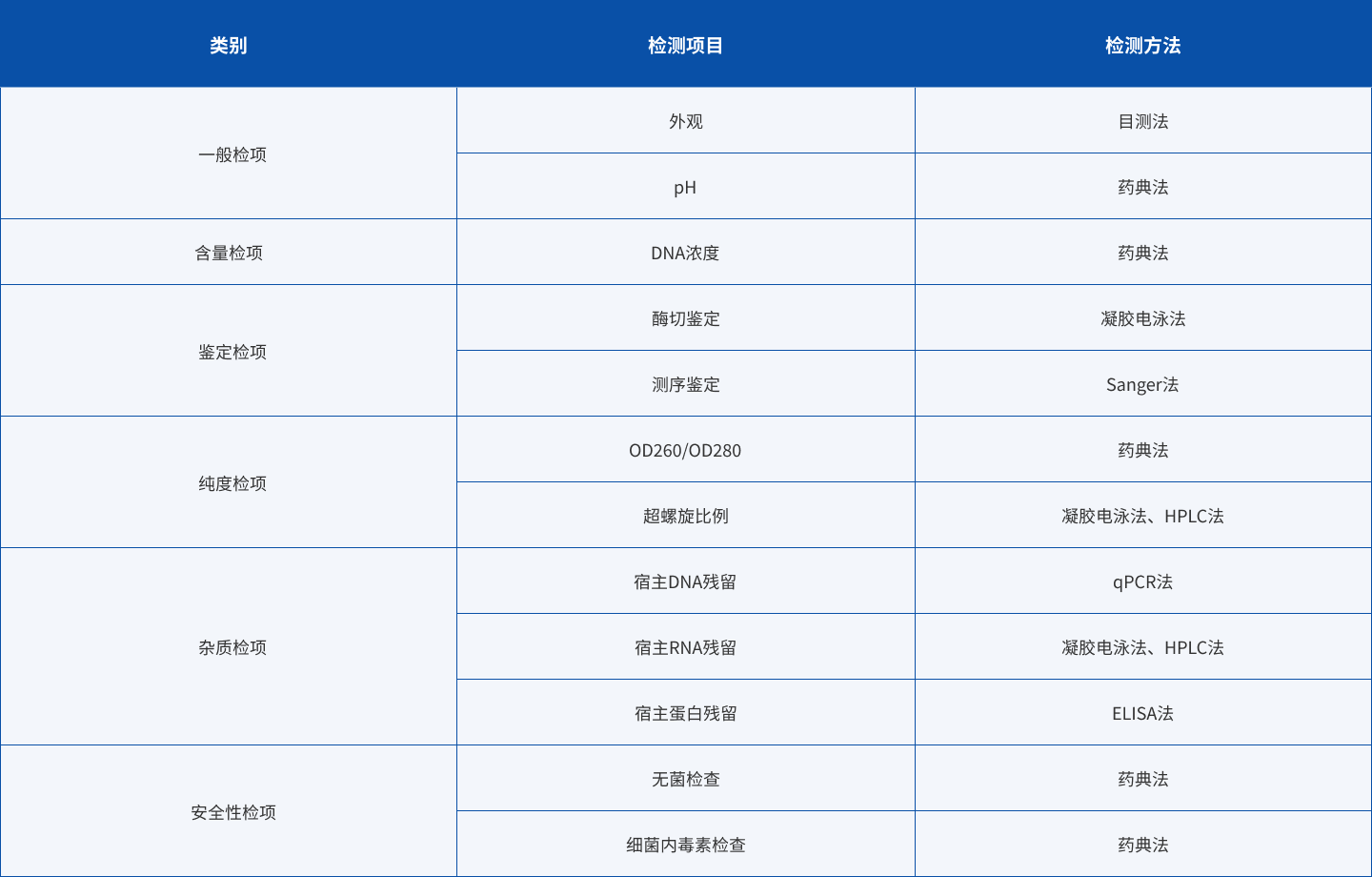
质粒作为细胞基因治疗最重要的原材料之一,既可用于病毒载体的组装并传递目的基因至宿主细胞内,也可在特定的生产工艺中作为终产品,直接用于细胞基因治疗。金检检测目前已经建立了以下质粒的质量控制分析方法:
慢病毒载体放行检项目
收起
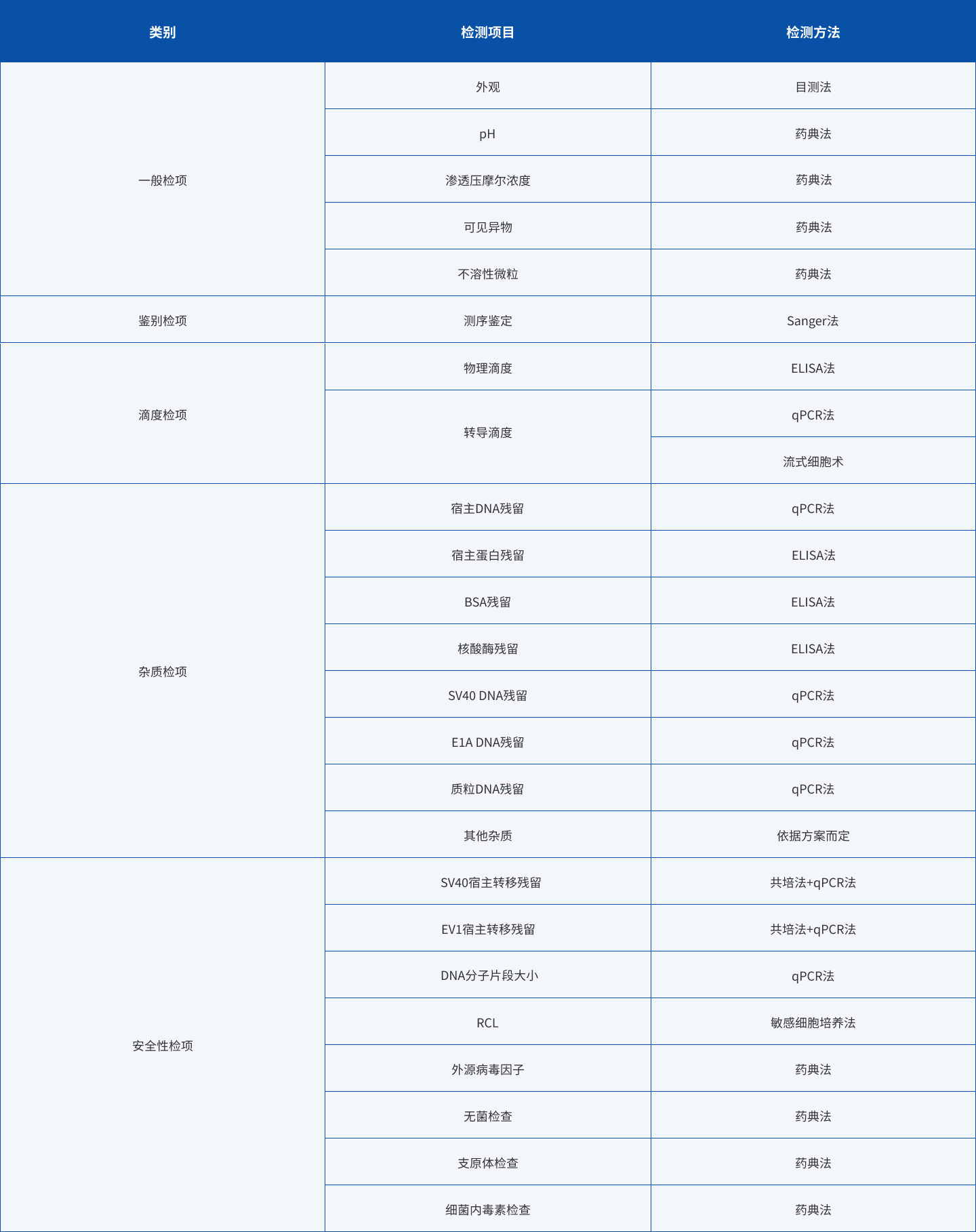
作为最主流最常用的病毒载体之一,慢病毒可以高效率将目的基因整合到宿主细胞的染色体上并长期稳定表达,可以有效地感染多种类型细胞,从而达到良好的细胞治疗效果。慢病毒载体被广泛的用于细胞治疗产品中,它的安全性和稳定生产也备受关注。金检检测目前已经建立了以下慢病毒载体的质量控制分析方法:
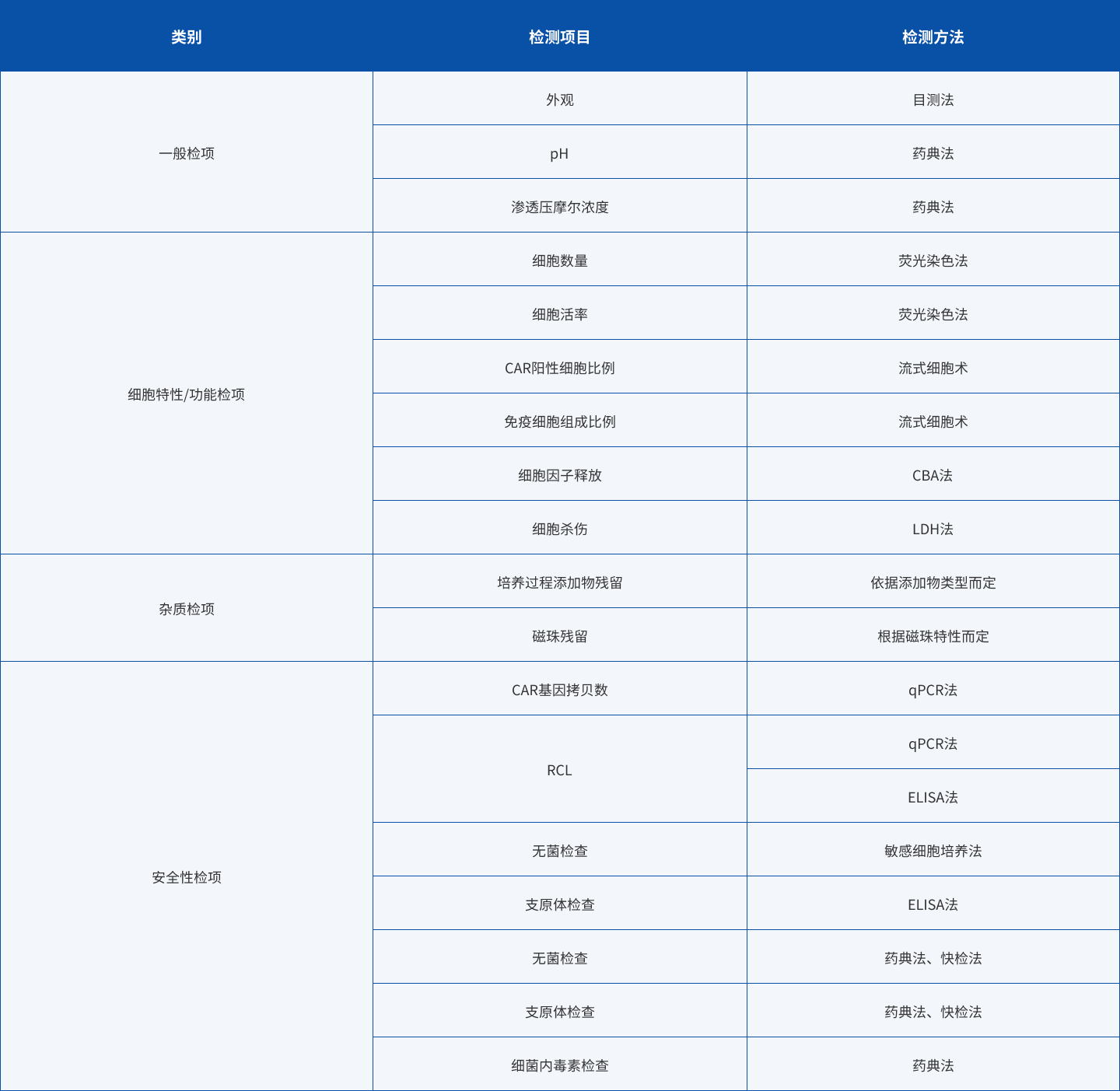
CAR-T细胞放行检项目
收起
CAR-T细胞,即嵌合抗原受体T细胞,属于免疫疗法中的一种,主要用于恶性血液病和恶性肿瘤患者的临床治疗。原理则是通过自身功能失效或不完全的T淋巴细胞,经过一定基因改造,装载上具有识别肿瘤抗原的受体及共刺激分子,通过在体外扩增后再次回输入患者体内,从而识别并攻击的能力,从而攻击自身的肿瘤细胞。金检检测目前已经建立了以下CART细胞的质量控制分析方法: